Su tesis doctoral, titulada "Rh(III)-catalyzed annulations based on C-H activation. Sustainable synthesis of carbo- and heterocycles", se basa en la utilización de un catalizador de rodio (III) capaz de romper enlaces C-H, con el fin de llevar a cabo reacciones de anillación oxidativa y generar eficientemente carbo- y heterociclos.
 El estudiante de doctorado Andrés Seoane Fernández ha defendido esta mañana su tesis doctoral titulada “Rh(III)-catalyzed annulations based on C-H activation. Sustainable synthesis of carbo- and heterocycles", supervisada por los investigadores del CiQUS José Luis Mascareñas y Moisés Gulías y orientada a la disminución de residuos generados durante la síntesis de moléculas complejas, uno de los retos principales de la química orgánica moderna.
El estudiante de doctorado Andrés Seoane Fernández ha defendido esta mañana su tesis doctoral titulada “Rh(III)-catalyzed annulations based on C-H activation. Sustainable synthesis of carbo- and heterocycles", supervisada por los investigadores del CiQUS José Luis Mascareñas y Moisés Gulías y orientada a la disminución de residuos generados durante la síntesis de moléculas complejas, uno de los retos principales de la química orgánica moderna.
Dentro de las aproximaciones más prometedoras para lograr este objetivo se encuentra la capacidad de funcionalizar directamente enlaces carbono-hidrógeno usando catálisis metálica. Estos procesos, conocidos como activación C-H, se pueden acoplar con etapas de anillación permitiendo obtener esqueletos cíclicos en pocas etapas a partir de sustratos sencillos y con una mínima generación de subproductos.
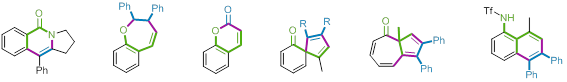
En este contexto, el principal objetivo de este trabajo, del que ya se publicaron varios resultados en revistas tan prestigiosas como J. Am. Chem. Soc., Angew. Chem. Int. Ed. o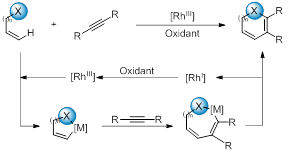 Chem. Sci, es la utilización de un catalizador de rodio (III) capaz de romper enlaces C-H para llevar a cabo reacciones de anillación oxidativa y generar eficientemente carbo- y heterociclos. Concretamente, se utilizaron benzamidas unidas a alquinos para obtener isoquinolinas tricíclicas y se descubrió que los o-alquenifenoles son sustratos versátiles frente a las reacciones de anillación, dando lugar a ciclos de cinco, seis y siete miembros como, benzoxepinas, cumarinas y azulenonas. Además, también se demostró que las o-alquenilanilidas son reactivas frente a este tipo de transformaciones permitiendo la síntesis de naftilaminas.
Chem. Sci, es la utilización de un catalizador de rodio (III) capaz de romper enlaces C-H para llevar a cabo reacciones de anillación oxidativa y generar eficientemente carbo- y heterociclos. Concretamente, se utilizaron benzamidas unidas a alquinos para obtener isoquinolinas tricíclicas y se descubrió que los o-alquenifenoles son sustratos versátiles frente a las reacciones de anillación, dando lugar a ciclos de cinco, seis y siete miembros como, benzoxepinas, cumarinas y azulenonas. Además, también se demostró que las o-alquenilanilidas son reactivas frente a este tipo de transformaciones permitiendo la síntesis de naftilaminas.