Martínez-Costas
Liñas de investigación
Investigador(es) principal/principais
Membros do grupo
| Barreiro Piñeiro, Natalia |
Inv. Posdoutoral |
|
| Abella López, Daniel |
Inv. Predoutoral |
|
| López Teijeiro, Adrián |
Inv. Predoutoral |
|
| Sánchez Gascón, Paula |
Inv. Predoutoral |
|
| Busch, Lisa Kay |
Inv. colaborador |
|
| Díaz Jullien, Cristina |
Inv. colaborador |
Investigación
Our laboratory was formerly dedicated to fundamental research on avian reoviruses (ARV). We have identified and characterized most of ARV proteins and determined many different steps of their replicative cycles. We have identified for the first time the existence of a functional tricistronic gene (S1 ARV gene) on a eukaryotic translation environment. Years ago, we focused on studying ARV morphogenesis that occurs inside membrane-less organelles called viroplasms and we were able to identify how the virus uses one single protein as scaffold (muNS) and stablished the correct and specific order in which all other viral components are recruited to those structures.
Based on those studies we have developed and patented an innovative protein micro- and nano-encapsulation platform based on the viral-derived muNS-Mi protein (a truncated version of muNS) that forms intracellular spheres within either prokaryotic or eukaryotic cells. We are currently involved if the development of this technology for its use in many different industrial and research applications, some of which are shown below. These spheres diameter range in size from micrometers (microspheres, MS, 1 to 4 μm) when produced in eukaryotes, to nanometers (nanospheres, NS, 300-400 nm) when produced in bacterial cells. They recruit in cellulo any protein carrying the so-called “Intercoil” tag (IC, 7kD) either at the N-terminus or C-terminus that co-exist in the same cell (Figure 1). MS or NS-encapsulated proteins maintain their native functionality, proper folding and quaternary interactions, allowing them to perform complex enzymatic reactions. In addition, encapsulated proteins get strongly stabilized against external stressors, such as pH variations, temperature or exposure to chemical agents, thereby preserving protein integrity.
This approach, combined with straightforward and a cost-effective purification method, makes this technology a highly versatile and efficient alternative for numerous applications. We have further developed and patented a new version of the methodology, MiST-IC Tagging, that allows the enzyme-mediated surface derivatization of the purified spheres with any molecule of choice, from small molecules (fluorophores, peptides, adjuvants…) to large substrates (proteins, affibodies, nanobodies…). Such covalent modification does not affect at all to the properties and activity of the encapsulated protein as is performed by an enzyme (Sortase A) that specifically recognizes the modified muNS-Mi protein (Figure 2).
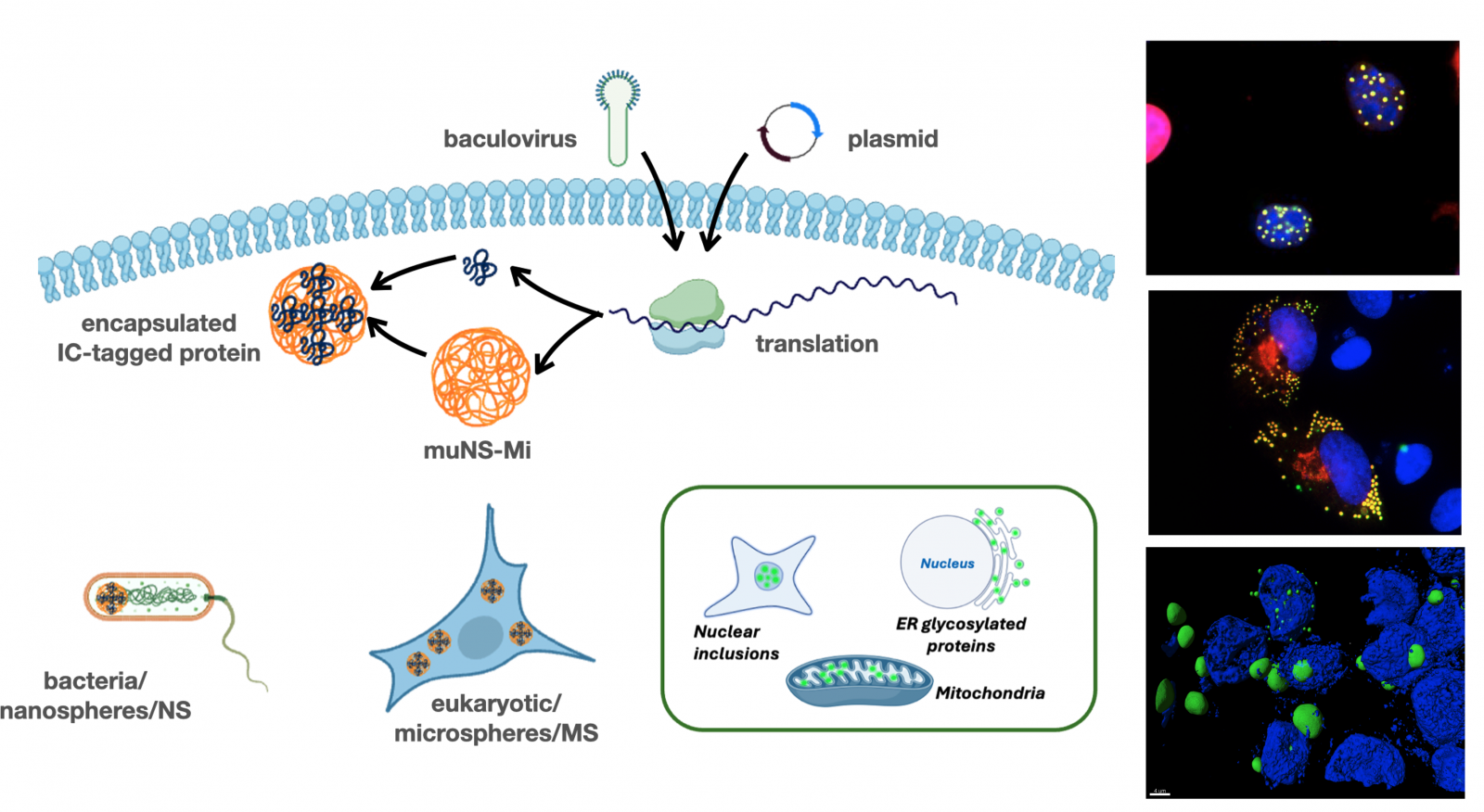 Figure 1. IC-Tagging explicative cartoon- Protein muNS-Mi forms spheres of micrometer (MS, eukaryotic) or nanometer (NS, prokaryotic) size, that recruits “in cellulo” any protein co-existing in the same cell, providing that it bears the IC tag. Versions that work inside the nucleus, ER or mitochondria are also available. Examples of nuclear (top), ER (middle) and baculovirus-produced MS are shown at the right.
Figure 1. IC-Tagging explicative cartoon- Protein muNS-Mi forms spheres of micrometer (MS, eukaryotic) or nanometer (NS, prokaryotic) size, that recruits “in cellulo” any protein co-existing in the same cell, providing that it bears the IC tag. Versions that work inside the nucleus, ER or mitochondria are also available. Examples of nuclear (top), ER (middle) and baculovirus-produced MS are shown at the right.
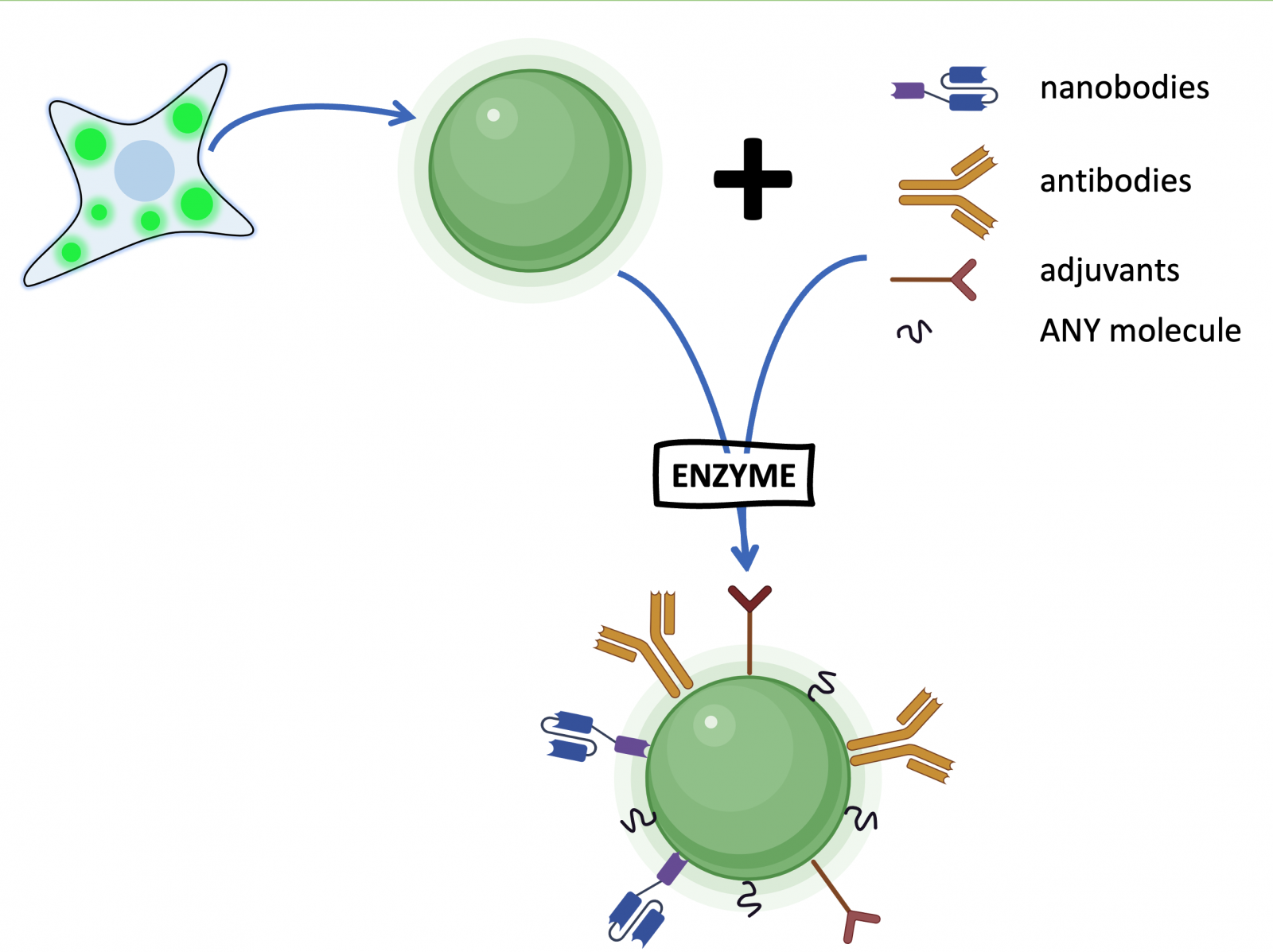 Figure 2. MiST-IC-Tagging- A modified protein muNS-Mi still forms spheres and works exactly as shown in figure 1, but it can be enzymatically modified after purification with any desired molecule without affecting the encapsulated protein
Figure 2. MiST-IC-Tagging- A modified protein muNS-Mi still forms spheres and works exactly as shown in figure 1, but it can be enzymatically modified after purification with any desired molecule without affecting the encapsulated protein
Production of subunit vaccines
IC or MiST-IC Tagging-produced spheres can be loaded with viral epitopes to generate safe, genome-free, subunit vaccines that need no adjuvant to produce a protective immune response. We have pre-clinically tested such vaccines for several viruses of veterinary (Figure 2, BTV, AHSV) and human (RVFV, CCHFV, SARS-CoV2) interest and some more (PRRSV, NNV) are being tested.
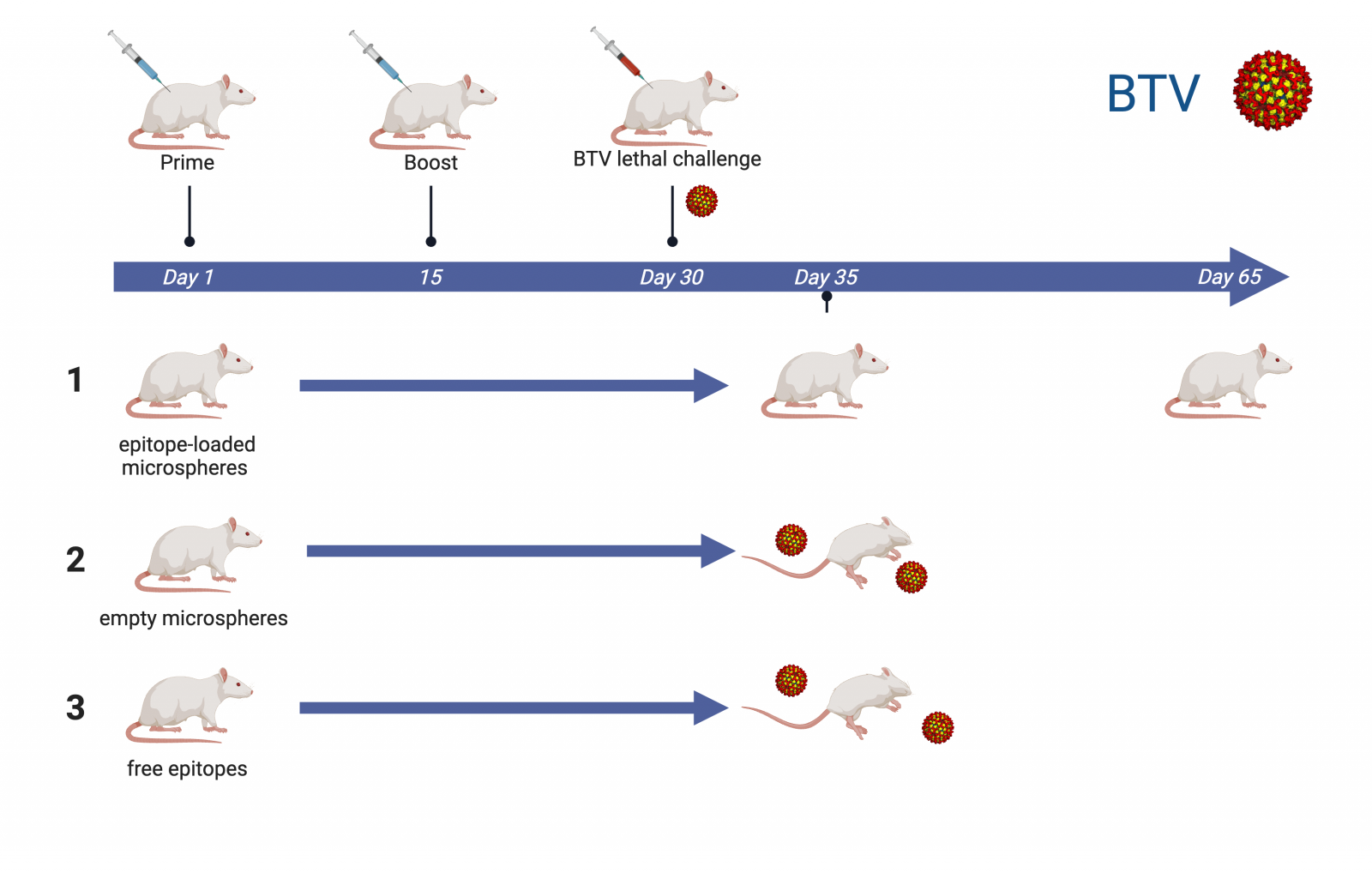 Figure 3. BTV preclinical trial using IC-Tagging-produced MS- Timeline of the prime-boost regime preclinical trial of a BTV vaccine using BTV epitope-loaded baculovirus-produced MS (1). As controls, empty MS (2) or free epitopes (3) were used. No adjuvant was added in any of the immunization groups. Five days post-challenge, both control groups died with a high viremia, while no effect was produced on the epitope-loaded MS-vaccinated group, that also presented no detectable virus in blood up to 30 days post-challenge.
Figure 3. BTV preclinical trial using IC-Tagging-produced MS- Timeline of the prime-boost regime preclinical trial of a BTV vaccine using BTV epitope-loaded baculovirus-produced MS (1). As controls, empty MS (2) or free epitopes (3) were used. No adjuvant was added in any of the immunization groups. Five days post-challenge, both control groups died with a high viremia, while no effect was produced on the epitope-loaded MS-vaccinated group, that also presented no detectable virus in blood up to 30 days post-challenge.
Enzyme stabilization
- Industrial application-
Laccase- We have produced a laccase with a much wider pH range than the free enzyme that is also strongly stabilized against denaturalization by chemical and physical factors. This enzyme resists incubations of 15 minutes at 95ºC or 30 minutes at 90ºC without affecting its activity. We found that such stabilization is typical from the immobilization inside our NS and thus we take advantage of it for many other applications and different enzyme developments. Some representative examples are mentioned below.
Nanoreactors- As several proteins can be simultaneously loaded inside the spheres, we actively work in the design and production of nanoreactors that perform different, complementary reactions. As an example, spheres containing peroxygenase and peroxide-producing enzymes are being generated.
Plastic recycling- We are developing different nano-encapsulated enzymes for the depolymerization of PET plastics (Figure 4). We are applying them to PET pellets, powder and post-consumer PET from fruit and nut containers, almost complete depolymerization in 72 hours with our immobilized enzyme. In addition, reutilization of the enzyme allows us to nearly full degrade two consecutive batches of plastic waste.
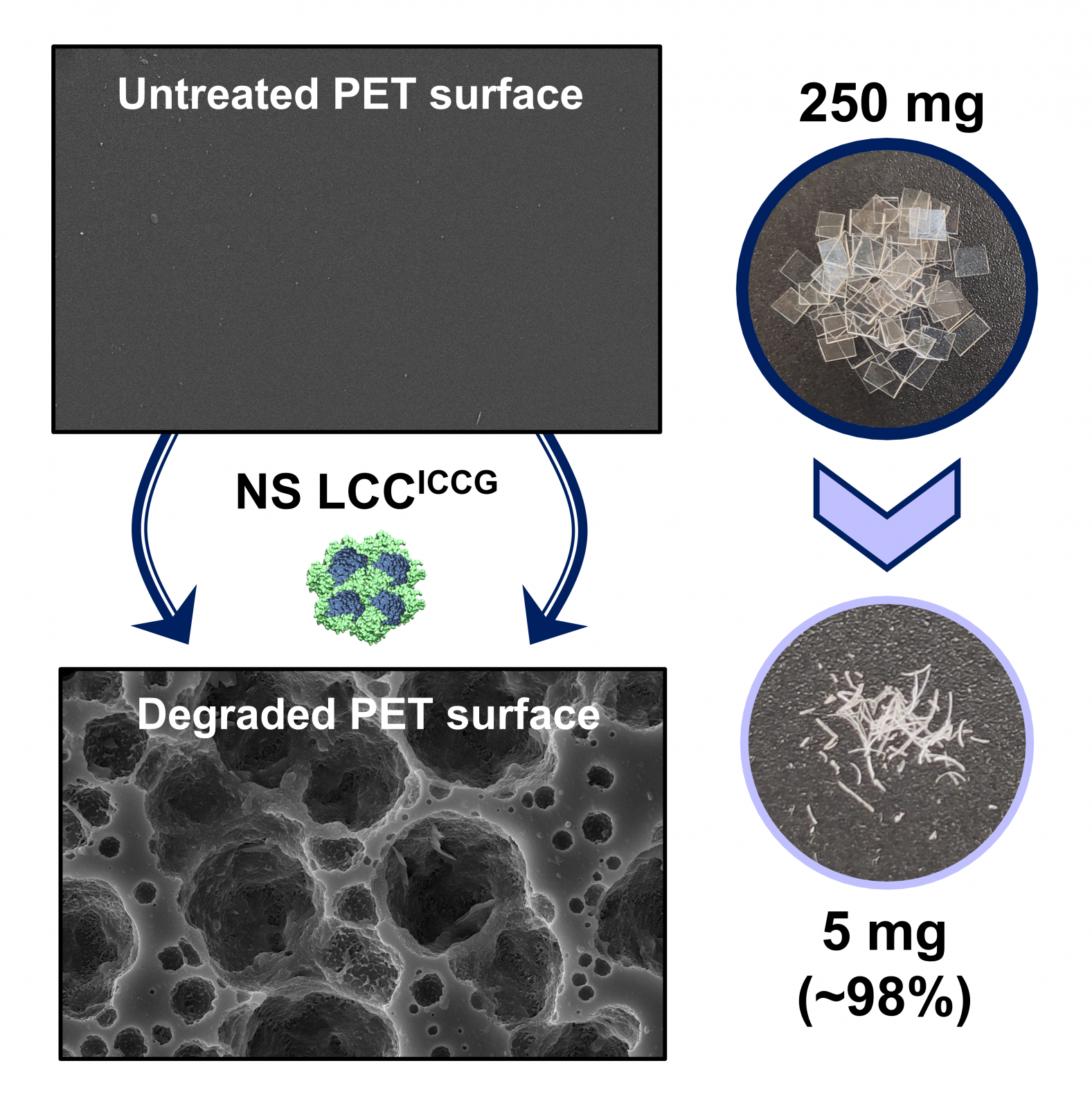 Figure 4. PET depolymerization using IC-Tagging-encapsulated enzymes- The pictures show the surface of PET pellets before (below) and after treating them with nano-encapsulated LCC-ICCG.
Figure 4. PET depolymerization using IC-Tagging-encapsulated enzymes- The pictures show the surface of PET pellets before (below) and after treating them with nano-encapsulated LCC-ICCG.
- Oral delivery of proteins for biomedical use-
Using this technology we have recently produced a nanosphere-encapsulated and chitosan-coated active form of AvPAL that is extremely resistant to acid pH and degradation by proteases. Furthermore, we studied the oral biodistribution and the resistance to the GI environment in vivo of a similarly nano-encapsulated and coated luciferase, whose activity was recovered intact in mice stomach, liver and feces, demonstrating that it remained active after full GI transit, while its activity was fully available (Figure 5). Thus, our technology represents a perfect tool for the oral delivery of peptides for many different purposes.




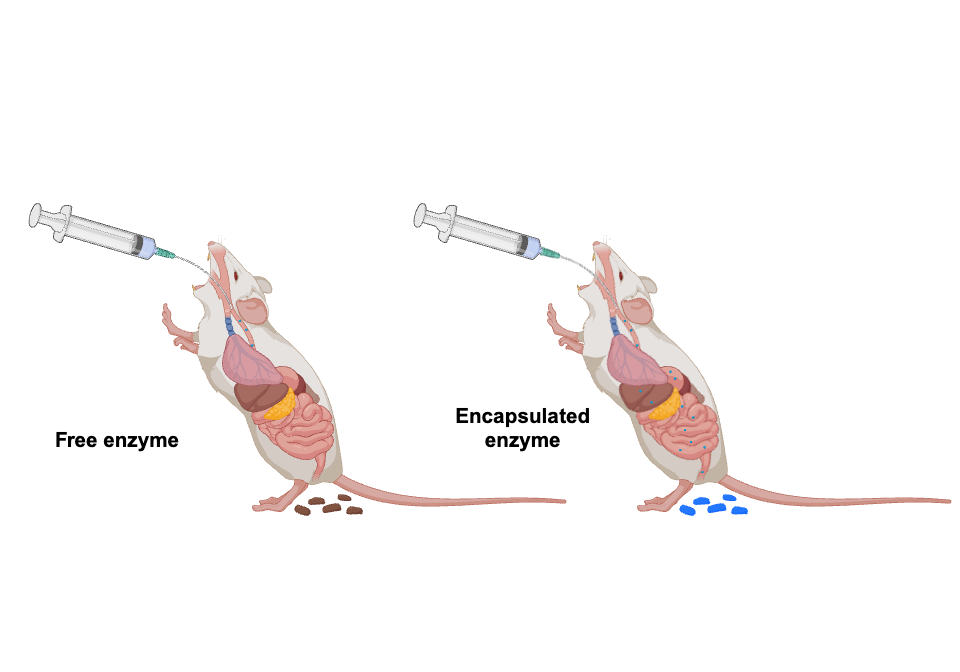 Figure 5. Gastrointestinal transit of IC-Tagging-encapsulated enzymes- After oral delivery, encapsulated enzymes resist the full gastrointestinal transit, even being perfectly active in mice feces.
Figure 5. Gastrointestinal transit of IC-Tagging-encapsulated enzymes- After oral delivery, encapsulated enzymes resist the full gastrointestinal transit, even being perfectly active in mice feces.